Zrak je sestavljen iz dušika. Revolucionarna sprememba sestave zraka
Zrak, ki sestavlja zemeljsko atmosfero, je mešanica plinov. Suh atmosferski zrak vsebuje: kisik 20,95%, dušik 78,09%, ogljikov dioksid 0,03%. Poleg tega atmosferski zrak vsebuje argon, helij, neon, kripton, vodik, ksenon in druge pline. V atmosferskem zraku so v majhnih količinah prisotni ozon, dušikov oksid, jod, metan in vodna para.
Poleg stalnih sestavin ozračja vsebuje različna onesnaževanja, ki jih v ozračje vnesejo človeške proizvodne dejavnosti.
1. Pomembna sestavina atmosferskega zraka je kisik , katerega količina v zemeljskem ozračju znaša 1,18 × 10 15 t. Konstantna vsebnost kisika se ohranja zaradi neprekinjenih procesov njegove izmenjave v naravi. Po eni strani se kisik porablja med dihanjem ljudi in živali, porabi se za vzdrževanje procesov zgorevanja in oksidacije, po drugi strani pa vstopa v ozračje zaradi procesov fotosinteze rastlin. Kopenske rastline in fitoplankton oceanov popolnoma obnovijo naravno izgubo kisika. Ob padcu parcialnega tlaka kisika se lahko razvijejo pojavi kisikovega stradanja, kar opazimo pri vzponu na višino. Kritična raven je parcialni tlak kisika pod 110 mm Hg. Umetnost. Zmanjšanje parcialnega tlaka kisika na 50-60 mm Hg. Umetnost. običajno nezdružljivo z življenjem. Pod vplivom kratkovalovnega UV sevanja z valovno dolžino manj kot 200 nm se molekule kisika disociirajo v atomski kisik. Novonastali atomi kisika se dodajo nevtralni formuli kisika in tvorijo ozona . Hkrati z nastankom ozona pride do njegovega razpada. Splošni biološki pomen ozona je velik: absorbira kratkovalovno UV sevanje, ki škodljivo vpliva na biološke objekte. Hkrati ozon absorbira infrardeče sevanje, ki prihaja iz Zemlje, in tako preprečuje prekomerno ohlajanje njene površine. Koncentracije ozona so neenakomerno razporejene po višini. Njegova največja količina je opažena na ravni 20-30 km od zemeljske površine.
2. dušik po kvantitativni vsebnosti je najpomembnejša sestavina atmosferskega zraka, spada med inertne pline. Življenje je v dušikovi atmosferi nemogoče. Zračni dušik asimilirajo nekatere vrste talnih bakterij (bakterije, ki vežejo dušik), pa tudi modro-zelene alge; pod vplivom električnih razelektritev se spremeni v dušikove okside, ki, ko izpadejo z atmosferskimi padavinami, obogatijo tla s solmi dušikove in dušikove kisline. Pod vplivom talnih bakterij se soli dušikove kisline pretvorijo v soli dušikove kisline, ki jih rastline absorbirajo in služijo za sintezo beljakovin. Skupaj z asimilacijo dušika v naravi se sprošča v ozračje. Prosti dušik nastane pri zgorevanju lesa, premoga, nafte; majhna količina nastane pri razgradnji organskih spojin. Tako v naravi obstaja neprekinjen cikel, zaradi katerega se dušik ozračja pretvori v organske spojine, obnovi in vstopi v ozračje, nato pa ga spet vežejo biološki predmeti.
Dušik je potreben kot razredčilo kisika, saj vdihavanje čistega kisika vodi do nepopravljivih sprememb v telesu.
Vendar pa povečana vsebnost dušika v vdihanem zraku prispeva k nastanku hipoksije zaradi zmanjšanja parcialnega tlaka kisika. S povečanjem vsebnosti dušika v zraku na 93% pride do smrti.
Poleg dušika inertni plini zraka vključujejo argon, neon, helij, kripton in ksenon. Kemično so ti plini inertni, v telesnih tekočinah se raztopijo glede na delni tlak, absolutna količina teh plinov v krvi in tkivih telesa je zanemarljiva.
3. Pomembna sestavina atmosferskega zraka je ogljikov dioksid (ogljikov dioksid, ogljikova kislina). V naravi je ogljikov dioksid v prostem in vezanem stanju v količini 146 milijard ton, od tega le 1,8% njegove celotne količine vsebuje atmosferski zrak. Večina (do 70%) je v raztopljenem stanju v vodah morij in oceanov. Nekatere mineralne spojine, apnenci in dolomiti vsebujejo okoli 22 % celotne količine dioksida in ogljika. Preostali del pade na živalski in rastlinski svet, premog, nafto in humus.
V naravnih razmerah potekajo neprekinjeni procesi sproščanja in absorpcije ogljikovega dioksida. V ozračje se sprošča zaradi dihanja ljudi in živali, procesov zgorevanja, razpadanja in fermentacije, pri industrijskem praženju apnenca in dolomitov itd. Hkrati v naravi potekajo procesi asimilacije ogljikovega dioksida, ki ga rastline absorbirajo v procesu fotosinteze.
Ogljikov dioksid ima pomembno vlogo v življenju živali in ljudi, saj je fiziološki povzročitelj dihalnega centra.
Pri vdihavanju visokih koncentracij ogljikovega dioksida se motijo redoks procesi v telesu. S povečanjem njegove vsebnosti v vdihanem zraku do 4% se opazijo glavoboli, tinitus, palpitacije in vznemirjeno stanje; pri 8 % pride do smrti.
S higienskega vidika je vsebnost ogljikovega dioksida pomemben kazalnik, po katerem ocenjujemo stopnjo čistosti zraka v stanovanjskih in javnih zgradbah. Kopičenje velikih količin v zraku v zaprtih prostorih kaže na sanitarne težave (gneče, slabo prezračevanje).
V normalnih pogojih z naravnim prezračevanjem prostorov in infiltracijo zunanjega zraka skozi pore gradbenih materialov vsebnost ogljikovega dioksida v zraku stanovanjskih prostorov ne presega 0,2%. S povečanjem njegove koncentracije v prostoru se lahko opazi poslabšanje dobrega počutja osebe, zmanjšanje delovne sposobnosti. To je razloženo z dejstvom, da se hkrati s povečanjem količine ogljikovega dioksida v zraku stanovanjskih in javnih zgradb poslabšajo tudi druge lastnosti zraka: povečata se njegova temperatura in vlažnost, pojavijo se plinasti produkti človekove vitalne dejavnosti, tako- imenovani antropotoksini (merkaptan, indol, vodikov sulfid, amoniak).
S povečanjem vsebnosti CO 2 v zraku in poslabšanjem meteoroloških razmer v stanovanjskih in javnih zgradbah se spremeni ionizacijski režim zraka (povečanje števila težkih in zmanjšanje števila lahkih ionov), kar je razloženo z absorpcijo lahkih ionov med dihanjem in stikom s kožo ter z vnosom težkih ionov z izdihanim zrakom.
Najvišja dovoljena koncentracija ogljikovega dioksida v zraku zdravstvenih ustanov je 0,07%, v zraku stanovanjskih in javnih zgradb - 0,1%. Slednja vrednost se vzame kot izračunana pri določanju učinkovitosti prezračevanja v stanovanjskih in javnih zgradbah.
4. Poleg glavnih sestavin atmosferski zrak vsebuje pline, ki se sproščajo kot posledica naravnih procesov, ki se pojavljajo na zemeljskem površju in v ozračju.
vodik v zraku v količini 0,00005%. Nastane v visokih plasteh ozračja zaradi fotokemične razgradnje molekul vode na kisik in vodik. Vodik ne podpira dihanja, v prostem stanju se ne absorbira in ga ne sproščajo biološki predmeti. Poleg vodika vsebuje atmosferski zrak majhno količino metana; običajno koncentracija metana v zraku ne presega 0,00022 %. Metan se sprošča med anaerobnim razpadom organskih spojin. Kot sestavni del je del zemeljskega plina in plina iz naftnih vrtin. Pri vdihavanju zraka, ki vsebuje metan v visokih koncentracijah, je možna smrt zaradi asfiksije.
Kot produkt razgradnje organskih snovi, majhne količine amoniak. Njegove koncentracije so odvisne od stopnje onesnaženosti območja s kanalizacijo in organskimi emisijami. Pozimi je zaradi upočasnitve procesov razpadanja koncentracija amoniaka nekoliko nižja kot poleti. Med anaerobnimi procesi razgradnje organskih snovi, ki vsebujejo žveplo, nastane vodikov sulfid, ki v nizkih koncentracijah daje zraku neprijeten vonj. V atmosferskem zraku lahko najdemo jod in vodikov peroksid v majhnih koncentracijah. jod vstopi v atmosferski zrak zaradi prisotnosti najmanjših kapljic morske vode in morskih alg. Zaradi interakcije UV-žarkov z molekulami zraka, vodikov peroksid; skupaj z ozonom prispeva k oksidaciji organskih snovi v ozračju.
V atmosferskem zraku so suspendirana snov, ki jih predstavlja prah naravnega in umetnega izvora. Sestava naravnega prahu vključuje kozmični, vulkanski, zemeljski, morski prah in prah, ki nastane ob gozdnih požarih.
Naravni procesi imajo pomembno vlogo pri sproščanju ozračja iz suspendiranih trdnih snovi. samočiščenje, med katerimi je zelo pomembno redčenje onesnaženja s konvekcijskimi zračnimi tokovi v bližini zemeljskega površja. Bistven element samočiščenja ozračja je obarjanje velikih delcev prahu in saj iz zraka (sedimentacija). Z naraščanjem nadmorske višine se količina prahu zmanjšuje; na višini 7 - 8 km od zemeljskega površja ni prahu zemeljskega izvora. Pomembna Padavine igrajo vlogo pri samočistilnih procesih, povečujejo količino usedlih saj in prahu. Na vsebnost prahu v atmosferskem zraku vplivajo meteorološke razmere in razpršenost aerosolov. Grobi prah s premerom delcev več kot 10 mikronov hitro pade ven, fin prah s premerom delcev manj kot 0,1 mikrona praktično ne pade ven in je v suspenziji.
Sestava zemlje. Zrak
Zrak je mehanska mešanica različnih plinov, ki sestavljajo Zemljino atmosfero. Zrak je bistven za dihanje živih organizmov in se pogosto uporablja v industriji.
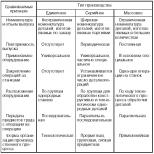
Dejstvo, da je zrak mešanica in ne homogena snov, je bilo dokazano med poskusi škotskega znanstvenika Josepha Blacka. Med enim od njih je znanstvenik odkril, da se pri segrevanju belega magnezijevega oksida (magnezijev karbonat) sprosti "vezan zrak", torej ogljikov dioksid, in nastane žgana magnezijeva (magnezijev oksid). Nasprotno pa se pri žganju apnenca odstrani "vezan zrak". Na podlagi teh poskusov je znanstvenik ugotovil, da je razlika med ogljikovimi in jedkimi alkalijami v tem, da prva vključuje ogljikov dioksid, ki je ena od sestavin zraka. Danes vemo, da poleg ogljikovega dioksida sestava zemeljskega zraka vključuje:
Razmerje plinov v zemeljski atmosferi, navedeno v tabeli, je značilno za njene nižje plasti, do višine 120 km. Na teh območjih leži dobro mešana, homogena regija, imenovana homosfera. Nad homosfero leži heterosfera, za katero je značilna razgradnja molekul plina na atome in ione. Regije so med seboj ločene s turbopavzo.
Kemična reakcija, pri kateri se pod vplivom sončnega in kozmičnega sevanja molekule razgradijo na atome, imenujemo fotodisocijacija. Med razpadom molekularnega kisika nastane atomski kisik, ki je glavni plin ozračja na nadmorskih višinah nad 200 km. Na višinah nad 1200 km začneta prevladovati vodik in helij, ki sta najlažja plina.
Ker je večina zraka koncentrirana v 3 nižjih atmosferskih plasteh, spremembe v sestavi zraka na višinah nad 100 km nimajo opaznega vpliva na celotno sestavo atmosfere.
Dušik je najpogostejši plin, ki predstavlja več kot tri četrtine zemeljske prostornine zraka. Sodobni dušik je nastal z oksidacijo zgodnje amoniak-vodikove atmosfere z molekularnim kisikom, ki nastane med fotosintezo. Trenutno majhna količina dušika vstopi v ozračje kot posledica denitrifikacije - procesa redukcije nitratov v nitrite, čemur sledi tvorba plinastih oksidov in molekularnega dušika, ki ga proizvajajo anaerobni prokarioti. Med vulkanskimi izbruhi nekaj dušika vstopi v ozračje.
V zgornji atmosferi, ko je izpostavljen električnim razelektritvam s sodelovanjem ozona, se molekularni dušik oksidira v dušikov monoksid:
N 2 + O 2 → 2NO
V normalnih pogojih monoksid takoj reagira s kisikom in tvori dušikov oksid:
2NO + O 2 → 2N 2 O
Dušik je najpomembnejši kemični element v zemeljski atmosferi. Dušik je del beljakovin, zagotavlja mineralno prehrano rastlin. Določa hitrost biokemičnih reakcij, igra vlogo razredčila kisika.
Kisik je drugi najpogostejši plin v Zemljini atmosferi. Nastajanje tega plina je povezano s fotosintetsko aktivnostjo rastlin in bakterij. In bolj raznoliki in številni fotosintetični organizmi so postajali, pomembnejši je postajal proces vsebnosti kisika v ozračju. Med razplinjevanjem plašča se sprosti majhna količina težkega kisika.
V zgornjih plasteh troposfere in stratosfere pod vplivom ultravijoličnega sončnega sevanja (označujemo ga kot hν) nastane ozon:
O 2 + hν → 2O
Zaradi delovanja istega ultravijoličnega sevanja ozon razpade:
O 3 + hν → O 2 + O
O 3 + O → 2O 2
Kot rezultat prve reakcije nastane atomski kisik, kot posledica druge - molekularni kisik. Vse 4 reakcije se imenujejo Chapmanov mehanizem, po britanskem znanstveniku Sidneyju Chapmanu, ki jih je odkril leta 1930.
Kisik se uporablja za dihanje živih organizmov. Z njegovo pomočjo se pojavijo procesi oksidacije in zgorevanja.
Ozon služi za zaščito živih organizmov pred ultravijoličnim sevanjem, ki povzroča nepopravljive mutacije. Najvišjo koncentracijo ozona opazimo v spodnji stratosferi znotraj t.i. ozonski plašč ali ozonski zaslon, ki leži na nadmorski višini 22-25 km. Vsebnost ozona je majhna: pri normalnem tlaku bi ves ozon zemeljske atmosfere zasedel plast debeline le 2,91 mm.
Nastajanje tretjega najpogostejšega plina v ozračju, argona, pa tudi neona, helija, kriptona in ksenona, je povezano z vulkanskimi izbruhi in razpadom radioaktivnih elementov.
Zlasti helij je produkt radioaktivnega razpada urana, torija in radija: 238 U → 234 Th + α, 230 Th → 226 Ra + 4 He, 226 Ra → 222 Rn + α (v teh reakcijah α- delec je helijevo jedro, ki v procesu izgube energije zajame elektrone in postane 4 He).
Argon nastane pri razpadu radioaktivnega izotopa kalija: 40 K → 40 Ar + γ.
Neon pobegne iz magmatskih kamnin.
Kripton nastane kot končni produkt razpada urana (235 U in 238 U) in torija Th.
Glavnina atmosferskega kriptona je nastala v zgodnjih fazah zemeljske evolucije kot posledica razpada transuranskih elementov s fenomenalno kratkim razpolovnim časom ali je prišel iz vesolja, v katerem je vsebnost kriptona deset milijonov krat večja kot na Zemlji. .
Ksenon je rezultat cepitve urana, vendar večina tega plina ostane iz zgodnjih stopenj nastanka Zemlje, iz primarne atmosfere.
Ogljikov dioksid vstopi v ozračje kot posledica vulkanskih izbruhov in v procesu razgradnje organske snovi. Njegova vsebnost v ozračju srednjih zemljepisnih širin se močno razlikuje glede na letne čase: pozimi se količina CO 2 poveča, poleti pa zmanjša. To nihanje je povezano z aktivnostjo rastlin, ki uporabljajo ogljikov dioksid v procesu fotosinteze.
Vodik nastane kot posledica razgradnje vode s sončnim sevanjem. Ker pa je najlažji plin, ki sestavlja ozračje, nenehno beži v vesolje, zato je njegova vsebnost v ozračju zelo majhna.
Vodna para je posledica izhlapevanja vode s površine jezer, rek, morij in kopnega.
Koncentracija glavnih plinov v nižjih plasteh ozračja, razen vodne pare in ogljikovega dioksida, je konstantna. V majhnih količinah atmosfera vsebuje žveplov oksid SO 2, amoniak NH 3, ogljikov monoksid CO, ozon O 3, vodikov klorid HCl, vodikov fluorid HF, dušikov monoksid NO, ogljikovodike, živosrebrove pare Hg, jod I 2 in mnoge druge. V spodnji atmosferski plasti troposfere je nenehno velika količina suspendiranih trdnih in tekočih delcev.
Viri trdnih delcev v zemeljskem ozračju so vulkanski izbruhi, cvetni prah rastlin, mikroorganizmi in v zadnjem času človeške dejavnosti, kot je kurjenje fosilnih goriv v proizvodnih procesih. Najmanjši delci prahu, ki so jedra kondenzacije, so vzroki za nastanek megle in oblakov. Brez trdnih delcev, ki so stalno prisotni v atmosferi, padavine ne bi padale na Zemljo.
Ne moreš se ga dotakniti, ne moreš ga videti in glavno, kar mu dolgujemo, je življenje. Seveda je to zrak, ki v folklori vsakega naroda ni zasedal zadnjega mesta. Kako so si ga predstavljali ljudje iz antike in kaj v resnici je - o tem bom pisal spodaj.
Plini, ki sestavljajo zrak
Naravna mešanica plinov imenovan zrak. Njegove potrebe in pomembnosti za življenje je težko podcenjevati – igra pomembno vlogo pri oksidativni procesi, ki jih spremlja sproščanje energije, potrebne za vsa živa bitja. S poskusi so znanstveniki lahko določili njegovo natančno sestavo, vendar je glavna stvar, ki jo je treba razumeti ni homogena snov, ampak mešanica plinov. Približno 99% sestave je mešanica kisika in dušika ter na splošno zrak tvori ozračje naš planet. Torej, mešanica je sestavljena iz naslednjih plinov:
- metan;
- kripton;
- helij;
- ksenon;
- vodik;
- neon;
- ogljikov dioksid;
- kisik;
- dušik;
- argon.

Treba je opozoriti, da sestava ni konstantna in se lahko od mesta do mesta močno razlikujejo. Za velika mesta je na primer značilna visoka vsebnost ogljikovega dioksida. V gorah bo opazovano zmanjšana raven kisika, saj je ta plin težji od dušika, in ko se dviga, se bo njegova gostota zmanjšala. Znanost pravi, da se lahko sestava v različnih delih planeta razlikuje 1% do 4% za vsak od plinov.

Poleg odstotka plinov so za zrak značilni naslednji parametri:
- vlažnost;
- temperatura;
- pritisk.
Zrak je nenehno v gibanju, ki tvorijo navpične tokove. Horizontalni - vetrovi so odvisni od določenih naravnih razmer, zato imajo lahko različne značilnosti hitrosti, moči in smeri.
Zrak v folklori
Legende vsakega naroda obdariti zrak z nekaterimi "bivalnimi" lastnostmi. Praviloma so bili duhovi tega elementa izmuzljiva in nevidna bitja. Po legendi so naseljenih gorskih vrhov ali oblakov, in se razlikujejo po nagnjenosti do osebe. Oni so bili tisti, ki so mislili ustvaril snežinke in zbral oblake v oblake, ki letijo po nebu na vetrove.

Egipčani so razmišljali o zraku simbol življenja in Indijanci so to verjeli izdih Brahme - življenje, in vdihavanje, oziroma smrt. Kar zadeva Slovane, je zrak (veter) zavzemal skoraj osrednje mesto v legendah tega ljudstva. Znal je slišati in včasih celo izpolniti majhne prošnje. Vendar ni bil vedno prijazen, včasih je govoril na strani sil zla. v obliki zlobnega in nepredvidljivega potepuha.
Zrak je bistven pogoj za življenje velikega števila organizmov na našem planetu.
Človek lahko živi en mesec brez hrane. Tri dni brez vode. Brez zraka - le nekaj minut.
Zgodovina raziskav
Vsi ne vedo, da je glavna sestavina našega življenja izjemno heterogena snov. Zrak je mešanica plinov. Kateri?
Dolgo časa je veljalo, da je zrak ena sama snov, ne mešanica plinov. Hipoteza o heterogenosti se je pojavila v znanstvenih delih mnogih znanstvenikov v različnih obdobjih. Toda nihče ni šel dlje od teoretičnih domnev. Šele v osemnajstem stoletju je škotski kemik Joseph Black eksperimentalno dokazal, da plinska sestava zraka ni enotna. Do odkritja je prišlo med rednimi poskusi.
Sodobni znanstveniki so dokazali, da je zrak mešanica plinov, sestavljena iz desetih osnovnih elementov.
Sestava se razlikuje glede na mesto koncentracije. Določanje sestave zraka poteka nenehno. Od tega je odvisno zdravje ljudi. Zrak je mešanica katerih plinov?
Na višjih legah (zlasti v gorah) je vsebnost kisika nizka. Ta koncentracija se imenuje "redek zrak". V gozdovih je, nasprotno, vsebnost kisika največja. V megamestih se poveča vsebnost ogljikovega dioksida. Določanje sestave zraka je ena najpomembnejših nalog okoljskih služb.
Kje se lahko uporablja zrak?
- Stisnjena masa se uporablja pri črpanju zraka pod tlakom. Montaža do deset barov je nameščena na kateri koli postaji za montažo pnevmatik. Pnevmatike so napolnjene z zrakom.
- Delavci uporabljajo odbojna kladiva, pnevmatske puške za hitro odstranjevanje / namestitev matic in vijakov. Za takšno opremo je značilna majhna teža in visoka učinkovitost.
- V industrijah, ki uporabljajo lake in barve, se uporablja za pospeševanje procesa sušenja.
- V avtopralnicah masa stisnjenega zraka pomaga pri hitrem sušenju avtomobilov;
- Proizvodni obrati uporabljajo stisnjen zrak za čiščenje orodja pred kakršno koli kontaminacijo. Na ta način lahko cele hangarje očistimo sekancev in žagovine.
- Petrokemična industrija si ne more več predstavljati brez opreme za čiščenje cevovodov pred prvim zagonom.
- Pri proizvodnji oksidov in kislin.
- Za dvig temperature tehnoloških procesov;
- Izvlečen iz zraka;
Zakaj živa bitja potrebujejo zrak?
Glavna naloga zraka, ali bolje rečeno, ene od glavnih sestavin - kisika - je prodreti v celice in s tem spodbujati oksidacijske procese. Zahvaljujoč temu telo prejme najpomembnejšo energijo za življenje.
Zrak vstopi v telo skozi pljuča, nato pa se po obtočnem sistemu porazdeli po telesu.
Zrak je mešanica katerih plinov? Poglejmo jih podrobneje.
dušik
Zrak je mešanica plinov, med katerimi je prvi dušik. Sedmi element periodičnega sistema Dmitrija Mendelejeva. Škotski kemik Daniel Rutherford leta 1772 velja za odkritelja.
Je del beljakovin in nukleinskih kislin človeškega telesa. Čeprav je njegov delež v celicah majhen – ne več kot tri odstotke, je plin nujen za normalno življenje.
V sestavi zraka je njegova vsebnost več kot oseminsedemdeset odstotkov.
V normalnih pogojih je brezbarven in brez vonja. Ne vstopa v spojine z drugimi kemičnimi elementi.
Največja količina dušika se uporablja v kemični industriji, predvsem v proizvodnji gnojil.
Dušik se uporablja v medicinski industriji, pri proizvodnji barvil,
V kozmetologiji se plin uporablja za zdravljenje aken, brazgotin, bradavic in telesnega termoregulacijskega sistema.
Z uporabo dušika se sintetizira amoniak, proizvaja dušikova kislina.
V kemični industriji se kisik uporablja za oksidacijo ogljikovodikov v alkohole, kisline, aldehide in za proizvodnjo dušikove kisline.
Ribiška industrija - oksigenacija rezervoarjev.
Toda najpomembnejši plin je za živa bitja. S pomočjo kisika lahko telo izkoristi (oksidira) potrebne beljakovine, maščobe in ogljikove hidrate ter jih pretvori v potrebno energijo.
Argon
Na tretjem mestu po pomembnosti je plin, ki je del zraka - argon. Vsebina ne presega enega odstotka. Je inerten plin brez barve, okusa in vonja. Osemnajsti element periodnega sistema.
Prva omemba je pripisana angleškemu kemiku leta 1785. Lord Laray in William Ramsay sta prejela Nobelovo nagrado za dokazovanje obstoja plina in eksperimente z njim.
Področja uporabe argona:
- žarnice z žarilno nitko;
- zapolnjevanje prostora med stekli v plastičnih oknih;
- zaščitno okolje med varjenjem;
- sredstvo za gašenje požara;
- za čiščenje zraka;
- kemična sinteza.
Za človeško telo ne koristi veliko. Pri visokih koncentracijah plina vodi do zadušitve.
Cilindri z argonom sive ali črne barve.
Preostalih sedem elementov predstavlja 0,03 % v zraku.
Ogljikov dioksid
Ogljikov dioksid v zraku je brez barve in vonja.
Nastane kot posledica razpadanja ali zgorevanja organskih materialov, sprošča se med dihanjem in delovanjem avtomobilov in drugih vozil.

V človeškem telesu nastaja v tkivih zaradi vitalnih procesov in se po venskem sistemu prenaša v pljuča.
Ima pozitiven pomen, ker pod obremenitvijo širi kapilare, kar zagotavlja možnost večjega transporta snovi. Pozitiven učinek na miokard. Pomaga povečati pogostost in moč obremenitve. Uporablja se za odpravo hipoksije. Sodeluje pri uravnavanju dihanja.
V industriji se ogljikov dioksid pridobiva iz produktov zgorevanja, kot stranski produkt kemičnih procesov ali pri separaciji zraka.
Aplikacija je izjemno široka:
- konzervans v živilski industriji;
- nasičenost pijač;
- gasilni aparati in gasilni sistemi;
- hranjenje akvarijskih rastlin;
- zaščitno okolje med varjenjem;
- uporaba v kartušah za plinsko orožje;
- hladilno sredstvo.
Neon
Zrak je mešanica plinov, od katerih je peti neon. Odprt je bil veliko pozneje - leta 1898. Ime je prevedeno iz grščine kot "novo".

Enoatomski plin, ki je brez barve in vonja.
Ima visoko električno prevodnost. Ima popolno elektronsko lupino. Inerten.
Plin se pridobi z ločevanjem zraka.
Aplikacija:
- Inertno okolje v industriji;
- Hladilno sredstvo v kriogenih napravah;
- Polnilo za plinske sijalke. Zahvaljujoč oglaševanju je našel široko uporabo. Večina barvnih napisov je narejenih z neonom. Ko preide električna razelektritev, svetilke dajo svetle barve.
- Signalne luči na svetilkah in letališčih. Dobro je deloval v močni megli.
- Element zračne mešanice za ljudi, ki delajo z visokim pritiskom.
helij
Helij je enoatomski plin, brez barve in vonja.

Aplikacija:
- Tako kot neon, ko električni razelektritev preide skozi, daje močno svetlobo.
- V industriji - za odstranjevanje nečistoč iz jekla med taljenjem;
- Hladilno sredstvo.
- Polnjenje zračnih ladij in balonov;
- Delno v dihalnih mešanicah za globoke potope.
- Hladilna tekočina v jedrskih reaktorjih.
- Glavno otroško veselje je letenje z baloni.
Za žive organizme to nima posebne koristi. V visokih koncentracijah lahko povzroči zastrupitev.
metan
Zrak je mešanica plinov, od katerih je sedmi metan. Plin je brez barve in vonja. Eksplozivno v visokih koncentracijah. Zato so mu za indikacijo dodane dišave.
Najpogosteje se uporablja kot gorivo in surovina v organski sintezi.
Domače peči, kotli, plinski grelniki vode delujejo predvsem na metan.
Produkt vitalne aktivnosti mikroorganizmov.
Kripton
Kripton je inerten enoatomski plin, brez barve in vonja.

Aplikacija:
- pri proizvodnji laserjev;
- oksidator pogonskega goriva;
- polnjenje žarnic z žarilno nitko.
Vpliv na človeško telo je bil malo raziskan. Preučujejo se aplikacije za globokomorsko potapljanje.
vodik
Vodik je brezbarven gorljiv plin.
Aplikacija:
- Kemična industrija - proizvodnja amoniaka, mila, plastike.
- Polnjenje sferičnih lupin v meteorologiji.
- Raketno gorivo.
- Hlajenje električnih generatorjev.
Xenon
Ksenon je enoatomski brezbarven plin.

Aplikacija:
- polnjenje žarnic z žarilno nitko;
- v motorjih vesoljskih plovil;
- kot anestetik.
Neškodljiv za človeško telo. Ne prinaša veliko koristi.
Majhni otroci pogosto sprašujejo starše, kaj je zrak in iz česa je običajno sestavljen. Vendar ne more vsak odrasel pravilno odgovoriti. Seveda so vsi preučevali zgradbo zraka v šoli pri naravoslovju, a z leti bi to znanje lahko pozabili. Poskusimo jih napolniti.
Kaj je zrak?
Zrak je edinstvena "snov". Ne moreš ga videti, se ga dotakniti, je brez okusa. Zato je tako težko jasno opredeliti, kaj je. Ponavadi samo rečejo – zrak je tisto, kar dihamo. Je povsod okoli nas, čeprav tega sploh ne opazimo. Začutite ga šele, ko zapiha močan veter ali se pojavi neprijeten vonj.
Kaj se zgodi, če zrak izgine? Brez tega ne more živeti in delovati noben živi organizem, kar pomeni, da bodo vsi ljudje in živali umrli. Za proces dihanja se ne zaobide. Pomembno je, kako čist in zdrav je zrak, ki ga vsi dihajo.

Kje lahko najdete svež zrak?
Najbolj uporaben zrak se nahaja:
- V gozdovih, zlasti borovih.
- V gorah.
- Blizu morja.
Zrak na teh mestih ima prijetno aromo in blagodejne lastnosti za telo. To pojasnjuje, zakaj se otroški zdravstveni kampi in različni sanatoriji nahajajo v bližini gozdov, v gorah ali na morski obali.
Na svežem zraku lahko uživate le stran od mesta. Zaradi tega mnogi ljudje kupujejo poletne koče zunaj vasi. Nekateri se preselijo v začasno ali stalno prebivališče v vasi, tam gradijo hiše. To še posebej velja za družine z majhnimi otroki. Ljudje odhajajo, ker je zrak v mestu močno onesnažen.

Problem onesnaženosti svežega zraka
V sodobnem svetu je problem onesnaženosti okolja še posebej aktualen. Delo sodobnih tovarn, podjetij, jedrskih elektrarn, avtomobilov negativno vpliva na naravo. V ozračje oddajajo škodljive snovi, ki onesnažujejo ozračje. Zato ljudje v urbanih območjih zelo pogosto občutijo pomanjkanje svežega zraka, kar je zelo nevarno.
Resna težava je težki zrak v slabo prezračevanem prostoru, še posebej, če so v njem računalniki in druga oprema. Ko je prisoten na takem mestu, se lahko človek začne dušiti zaradi pomanjkanja zraka, ima bolečino v glavi, pojavi se šibkost.
Po statističnih podatkih, ki jih je zbrala Svetovna zdravstvena organizacija, je približno 7 milijonov človeških smrti na leto povezanih z absorpcijo onesnaženega zraka na ulici in v zaprtih prostorih.
Škodljiv zrak velja za enega glavnih vzrokov za tako grozno bolezen, kot je rak. Tako pravijo organizacije, ki se ukvarjajo s preučevanjem raka.
Zato je treba sprejeti preventivne ukrepe.

Kako do svežega zraka?
Človek bo zdrav, če bo lahko vsak dan dihal svež zrak. Če se zaradi pomembnega dela, pomanjkanja denarja ali drugih razlogov ni mogoče preseliti iz mesta, potem je treba sproti iskati izhod iz situacije. Da bi telo dobilo potrebno normo svežega zraka, je treba upoštevati naslednja pravila:
- Da bi bili pogosteje na ulici, na primer, da bi hodili zvečer po parkih, vrtovih.
- Ob vikendih pojdite na sprehod v gozd.
- Nenehno zračite bivalne in delovne prostore.
- Posadite več zelenih rastlin, zlasti v pisarnah, kjer so računalniki.
- Priporočljivo je, da enkrat letno obiščete letovišča na morju ali v gorah.

Iz katerih plinov je sestavljen zrak?
Vsak dan, vsako sekundo ljudje vdihnejo in izdihnejo, popolnoma brez razmišljanja o zraku. Ljudje se nanj nikakor ne odzovejo, kljub temu, da jih povsod obkroža. Kljub breztežnosti in nevidnosti za človeško oko ima zrak precej zapleteno strukturo. Vključuje medsebojno razmerje več plinov:
- dušik.
- Kisik.
- Argon.
- Ogljikov dioksid.
- Neon.
- metan.
- helij.
- Kripton.
- vodik.
- Xenon.
Glavni del zraka je dušik , katerega masni delež je 78 odstotkov. 21 odstotkov vsega je kisik, ki je najpomembnejši plin za človeško življenje. Preostale odstotke zasedajo drugi plini in vodna para, iz katerih nastanejo oblaki.
Lahko se pojavi vprašanje, zakaj je kisika tako malo, le nekaj več kot 20 %? Ta plin je reaktiven. Zato se bo s povečanjem njegovega deleža v ozračju verjetnost požarov na svetu močno povečala.

Iz česa je sestavljen zrak, ki ga dihamo?
Dva glavna plina, ki sestavljata osnovo zraka, ki ga dihamo vsak dan, sta:
- Kisik.
- Ogljikov dioksid.
Vdihavamo kisik, izdihujemo ogljikov dioksid. Vsak študent pozna te podatke. Toda od kod prihaja kisik? Glavni vir proizvodnje kisika so zelene rastline. So tudi potrošniki ogljikovega dioksida.
Svet je zanimiv. V vseh tekočih življenjskih procesih se upošteva pravilo ohranjanja ravnovesja. Če je nekaj od nekod šlo, potem je nekaj nekje prišlo. Tako je tudi z zrakom. Zelene površine proizvajajo kisik, ki ga človeštvo potrebuje za dihanje. Ljudje sprejemamo kisik in oddajamo ogljikov dioksid, ki ga nato uporabljajo rastline. Zahvaljujoč temu sistemu interakcije na planetu Zemlja obstaja življenje.
Če vemo, iz česa je sestavljen zrak, ki ga dihamo, in koliko je onesnažen v sodobnem času, je treba zaščititi floro planeta in narediti vse, da povečamo predstavnike zelenih rastlin.
Video o sestavi zraka